INVESTOR RELATIONS
News
 > INVESTOR RELATIONS > News
> INVESTOR RELATIONS > News
| 나이벡, 치주조직 재생 콜라겐 바이오소재 중국 180명 대상 시술 완료 | ||
|---|---|---|
|
||
|
나이벡, 치주조직 재생 콜라겐 바이오소재 중국 180명 대상 시술 완료 ▶ 180명대상 시술완료 현재 관찰 중 ▶ 골재생 바이오소재인 OCS-B 는 임상시험 완료 후 중국 식약처 1차 대면 보완
[2019-04-25] 나이벡(대표이사 정종평)은 현재 중국에서 임상시험 중인 자사 제품 치주조직 재생콜라겐 바이오소재인 <GuidOss> 차폐막에 대한 환자 시술을 완료했다고 25일 밝혔다.
나이벡은 소뼈에서 추출한 치과용 골재생 바이오소재인 OCS-B에 이어 치주조직재생 콜라겐 바이오 소재인 가이도스(GuidOss) 차폐막에 대해서도 중국 판매허가를 위한 임상시험을 진행 중이라고 설명했다.
나이벡 관계자는 “총 180명 환자에게 시술을 완료했으며 현재 종합적으로 관찰중”이라며 “2년 전부터 진행해온 임상시험으로 대부분의 환자들로부터 제품에 대한 유효성은 이미 확보한 상태”라고 말했다.
회사는 올 하반기 최종 임상시험 완료를 목표로 두고 있으며, 내년 상반기에는 중국 식약처에 판매허가신청서를 제출할 계획이다.
한편, 소뼈 유래 치과용 골재생 바이오소재인 OCS-B의 경우 지난 1월 판매허가를 신청해 추가 서류제출 및 마무리단계에 접어든 것으로 보인다.
회사는 이미 한국을 비롯한 유럽, 미국 등 전 세계적으로 제품을 공급판매하고 있기 때문에 중국에서도 중국 또한 품목허가 취득이 차질없이 진행될 것으로 예상하고 있다고 설명했다.
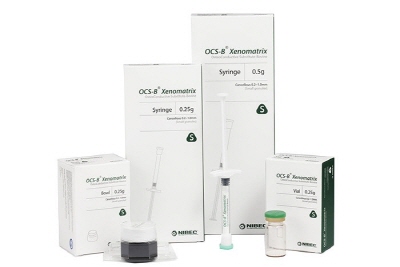
<중국 판매허가 심의중인 OCS-B제품(좌), 임상시험 시술 완료한 GuidOss(우)>
실제로, 나이벡의 소뼈 유래 치과용 골이식재인 ‘OCS-B’와 ‘GuidOss’는 나이벡의 주요 매출 비중을 차지하는 제품으로 글로벌 임플란트 회사인 스트라우만과 노벨바이오케어를 통해 유럽, 미국 등 글로벌 지역으로 수출하고 있다.
나이벡 관계자는 “OCS-B의 중국 판매허가 신청과 가이도스(GuidOss)의 임상 시술 등은 중국시장 진출의 신호탄으로서 큰 의미가 있다”며 “글로벌 기업들로부터 인정받은 제품기술력을 바탕으로 중국 시장으로 신속히 진입할 수 있도록 노력중”이라고 덧붙였다. |
||
| 이전글 | 나이벡, 글로벌 제약사들과 JP Morgan 헬스 컨퍼런스 후속 미팅 진행 | |
| 다음글 | 나이벡, 바이오 세계 최대 컨퍼런스 ''바이오 USA'' 초청 발표 | |